Una campagna vaccinale in continua, inevitabile, evoluzione richiede un importante sforzo comunicativo e un confronto altrettanto continuo.
Per questo motivo AIFA organizza una serie di appuntamenti periodici, con cadenza quindicinale, dedicati all’approfondimento scientifico e al confronto sulle scelte, uno spazio che offra la possibilità di illustrare più in dettaglio le ragioni e il percorso delle decisioni prese da AIFA e di discuterne le ricadute insieme a chi è chiamato a gestirle e metterle in pratica nel nostro SSN. L’obiettivo è anche quello di fornire un ulteriore strumento, che vada ad integrarsi con quanto già AIFA offre in termini di strumenti informativi (la documentazione pubblicata sul sito istituzionale, le FAQ, il Rapporto mensile sulla sorveglianza dei vaccini COVID-19), costruendo uno spazio reale di condivisione, di ascolto e dialogo. Saranno comunque affrontati di volta in volta anche i temi di più stretta attualità.
Il primo appuntamento è previsto per giovedì 4 marzo 2021 dalle 16 alle 18 e sarà accessibile sul canale YouTube di AIFA attraverso il link https://youtu.be/QfMSzVfFmeU.
Il seminario non è aperto alla stampa!
Di seguito il programma dei lavori, che saranno coordinati dalla Dott.ssa Eva Benelli (Comitato Scientifico per la sorveglianza post-marketing dei Vaccini Covid-19):
Nicola Magrini (Direttore Generale AIFA) – Perché siamo qui
Vittorio Demicheli (Comitato Scientifico per la sorveglianza post-marketing dei Vaccini Covid-19) – I tre vaccini in ottica di sanità pubblica
Maria Rosa Valetto (medico vaccinatore) – Cronache dalla prima linea, tre aspetti affrontati nelle FAQ AIFA: vaccinazione in allattamento, vaccinare i guariti?, perché e fino a quando distanziare il richiamo
Discussione: Angela Giusti (Istituto Superiore di Sanità), Guido Forni (Comitato Scientifico per la sorveglianza post-marketing dei Vaccini Covid-19), Patrizia Popoli (Commissione Tecnico Scientifica AIFA)
Anna Lisa Mandorino (Cittadinanzattiva) – Storie della società civile
Domenico Martinelli (Regione Puglia) – Possiamo dire di aver davvero terminato la prima fase della campagna vaccinale?
Discussione e conclusioni



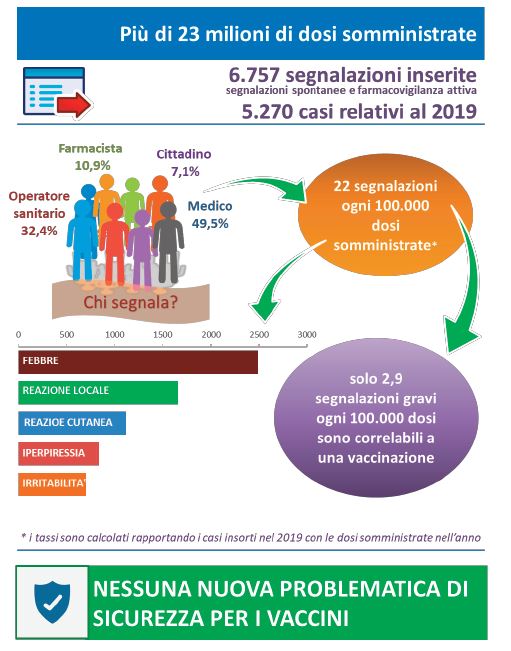
 Un gruppo di ricercatori italiani afferenti all’Università di Verona in collaborazione con l’Agenzia Italiana del Farmaco ha utilizzato il Sistema Italiano di Farmacovigilanza per analizzare le reazioni avverse ai vaccini riportate in un periodo di 10 anni (2008 – 2017).
Un gruppo di ricercatori italiani afferenti all’Università di Verona in collaborazione con l’Agenzia Italiana del Farmaco ha utilizzato il Sistema Italiano di Farmacovigilanza per analizzare le reazioni avverse ai vaccini riportate in un periodo di 10 anni (2008 – 2017).