Pubblicato online il Bollettino News del Centro Regionale di Farmacovigilanza Sardegna di luglio 2020, in cui si descrive lo stato dell’arte sulla ricerca in corso nell’ambito del COVID-19 in quanto a sperimentazioni cliniche e vaccini.
Pubblicato online il Bollettino News del Centro Regionale di Farmacovigilanza Sardegna di luglio 2020, in cui si descrive lo stato dell’arte sulla ricerca in corso nell’ambito del COVID-19 in quanto a sperimentazioni cliniche e vaccini.
Covid-19 e sperimentazioni cliniche: stato dell’arte
Durante la pandemia da COVID-19, AIFA si è occupata di garantire l’accesso alle cure al maggior numero possibile di pazienti e allo stesso tempo di prevenire un uso inappropriato dei farmaci e ridurre il rischio di effetti avversi.
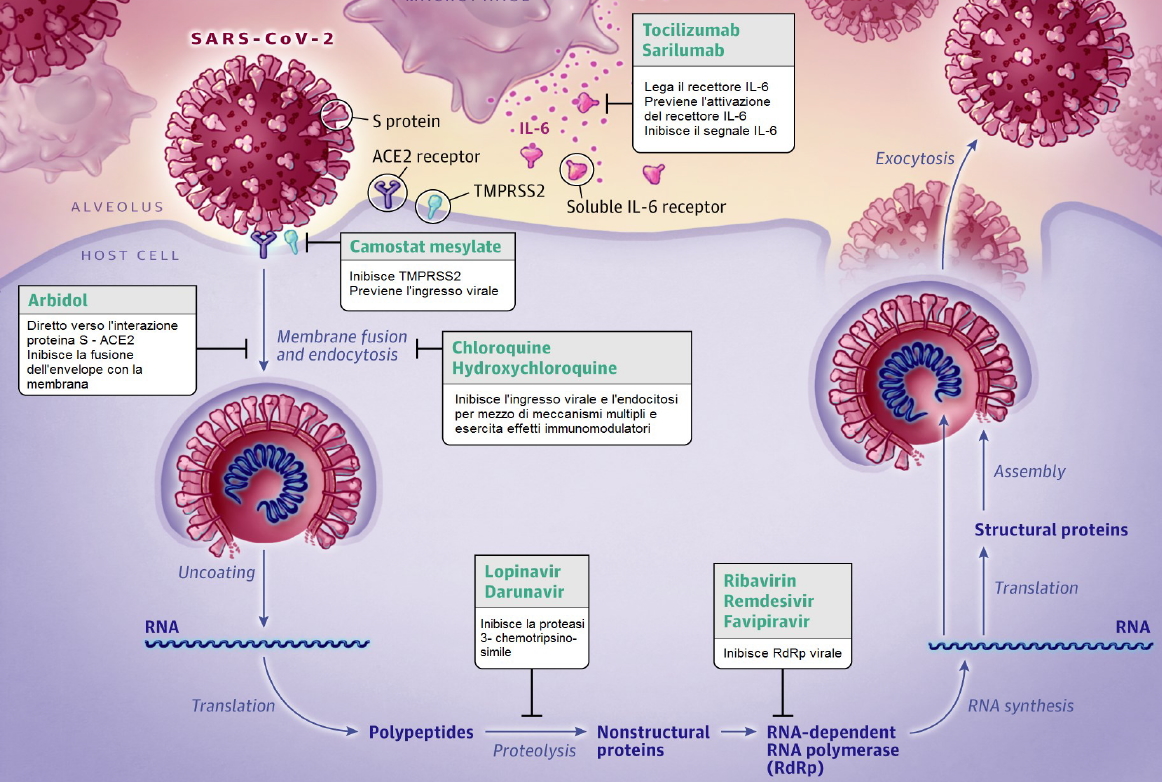
Diversi farmaci autorizzati per altre patologie sono entrati in uso off-label nella pratica clinica per trattare i pazienti colpiti da Covid-19, fino a diventarne lo standard di cura, nonostante la scarsità di dati a favore della loro efficacia. Tra questi:
- l’antireumatico idrossilammina,
- gli antivirali lopinavir/ritonavir e darunavir/cobicistat,
- l’antibiotico azitromicina, e
- le eparine a basso peso molecolare.
Tra i farmaci oggetto di studio l’idrossiclorochina ha riscosso molto successo al punto da essere inclusa in ben 5 sperimentazioni in Italia. Tuttavia, nonostante i risultati promettenti in vitro, non ha finora dimostrato maggiore efficacia rispetto al placebo nel ridurre il rischio di ospedalizzazione nei pazienti con sintomi moderati o nell’abbreviare il tempo di risoluzione dei sintomi.
Oltre a farmaci che contrastano direttamente l’infezione virale, particolare attenzione è stata posta sulla flogosi, che nell’infezione da SARS-CoV-2 sembra svolgere un ruolo fondamentale. Il virus induce infatti una risposta immunitaria dell’ospite eccessiva e aberrante associata ad una grave polmonite interstiziale potenzialmente letale. In molti pazienti, soprattutto nelle forme gravi di malattia, l’infezione è associata ad una “tempesta citochinica”, un incremento delle concentrazioni plasmatiche di numerose citochine che sembra rappresentare uno dei più importanti fattori prognostici negativi.
Fin da subito l’attenzione si è concentrata sul tocilizumab, anticorpo monoclonale diretto contro il recettore umano dell’interleuchina 6 (IL-6), già in uso in ambito reumatologico. Altre potenziali strategie terapeutiche si basano sulla modulazione su più punti delle diverse tappe della cascata citochinica responsabile della tempesta infiammatoria, quali la via dell’interleuchina-1, quella dell’interferone-ɤ e molti altri siti di azione (per una disamina più approfondita si rimanda al testo completo).
Covid-19 e vaccini: una nuova sfida per regolatorio e industria
La recente pandemia da Covid-19 ha attivato sforzi senza precedenti da parte di istituzioni e aziende per velocizzare la ricerca di un possibile vaccino e sostenerne i costi. Dalla bozza pubblicata dall’OMS il 15 luglio 2020, a pochi mesi dall’isolamento di Covid-19, sono già oltre 140 i vaccini in fase preclinica e ben 23 quelli già arrivati, in tempi record, alla fase clinica. Si tratta di progetti di grandi e piccole industrie, ma anche, per circa un terzo, di gruppi di ricerca no-profit.
La corsa ai vaccini anti SARS-CoV-2 ha posto una serie di sfide alla sperimentazione clinica. Problemi etici sono emersi, ad esempio, dai cosiddetti Human Challenge Trials, ossia la strategia di inoculare il virus in volontari sani in seguito alla somministrazione del vaccino, e di cui l’OMS aveva già predisposto linee guida.
 Inoltre, il percorso che porta alla approvazione di un vaccino è lungo e tortuoso: come ricorda il CEO di Merck, sono solo 7 i veri nuovi vaccini sviluppati negli ultimi 25 anni da aziende private, e tutti hanno richiesto un lungo periodo di tempo prima della approvazione. Il più recente vaccino contro il virus Ebola ha richiesto ben 5 anni e mezzo.
Inoltre, il percorso che porta alla approvazione di un vaccino è lungo e tortuoso: come ricorda il CEO di Merck, sono solo 7 i veri nuovi vaccini sviluppati negli ultimi 25 anni da aziende private, e tutti hanno richiesto un lungo periodo di tempo prima della approvazione. Il più recente vaccino contro il virus Ebola ha richiesto ben 5 anni e mezzo.
L’urgenza di avere un’arma efficace non può prescindere da una rigorosa raccolta e valutazione dei dati: un opinion paper pubblicato su JAMA ci ricorda amaramente come nel 1955, in seguito alle pressioni per un rilascio tempestivo del vaccino anti-polio Salk, la sua produzione accelerata e non supervisionata ha portato alla distribuzione di un vaccino contaminato con poliovirus vivo e alla paralisi di oltre 100 bambini.
È inoltre necessario garantire una sufficiente efficacia e una durata dell’immunizzazione nel tempo quando sono ancora poche le conoscenze sul funzionamento di SARS-CoV-2.
Se la sfida di sviluppare un vaccino efficace e sicuro entro il 2021 sarà vinta, questo segnerà un traguardo inedito nella sperimentazione clinica, per tempistiche, sforzi e sinergie messe in campo da pubblico e privato.
Scarica il Bollettino formato PDF, oppure consulta la pagina con i tutti i bollettini.